- »
- Recherche »
- Recherche Clinique
L’INSTITUT GODINOT ET LA RECHERCHE CLINIQUE
Directeur de la Recherche clinique : Dr. Jean-Christophe EYMARD

Qu'est ce que la recherche clinique ?
La recherche clinique, ou essais cliniques, est une étape incontournable du développement d’un produit de santé avant sa mise sur le marché. Elle vise à démontrer que le candidat médicament est efficace et que ses effets indésirables éventuels ne sont pas trop importants ; c’est ce qu’on appelle le rapport bénéfice / risque qui est évalué par l’Agence du Médicament qui accordera ou non une Autorisation de Mise sur le Marché (AMM).
Démarche qualité :
La certification de la Recherche clinique selon la norme ISO 9001 : 2015 a été reconduite le 12 mai 2020 (N° de certificat : 201051/1484F) pour le périmètre d’investigation (étude de faisabilité et mise en place de l’étude, gestion des inclusions et suivi des patients, gestion des données associées, clôture de l’étude clinique).
Cette certification garantit la qualité de la prise en charge des patients inclus dans les essais cliniques mis en place au sein de l’institut Godinot.
À quoi sert la recherche clinique contre le cancer ?
La recherche clinique constitue une des missions prioritaires des CLCC parallèlement aux soins des patients porteurs de cancer. Cette activité est indispensable pour l’amélioration des thérapeutiques anti-cancéreuses. Un essai clinique a pour objectif de s’assurer qu’un nouveau traitement est plus efficace que celui de référence et qu’il est bien toléré, ou parfois qu’il est aussi efficace mais mieux toléré. En cancérologie, on évalue ainsi les nouvelles molécules, les essais cliniques chez l’Homme se déroulent en 3 phases. Si, à l’une des phases de développement, il apparaît des doutes quant à l’efficacité ou la sécurité d’emploi du futur médicament, les essais cliniques sont arrêtés et la recherche s’interrompt définitivement. Seuls les candidats médicaments qui passent les différentes phases avec succès sont mis sur le marché.
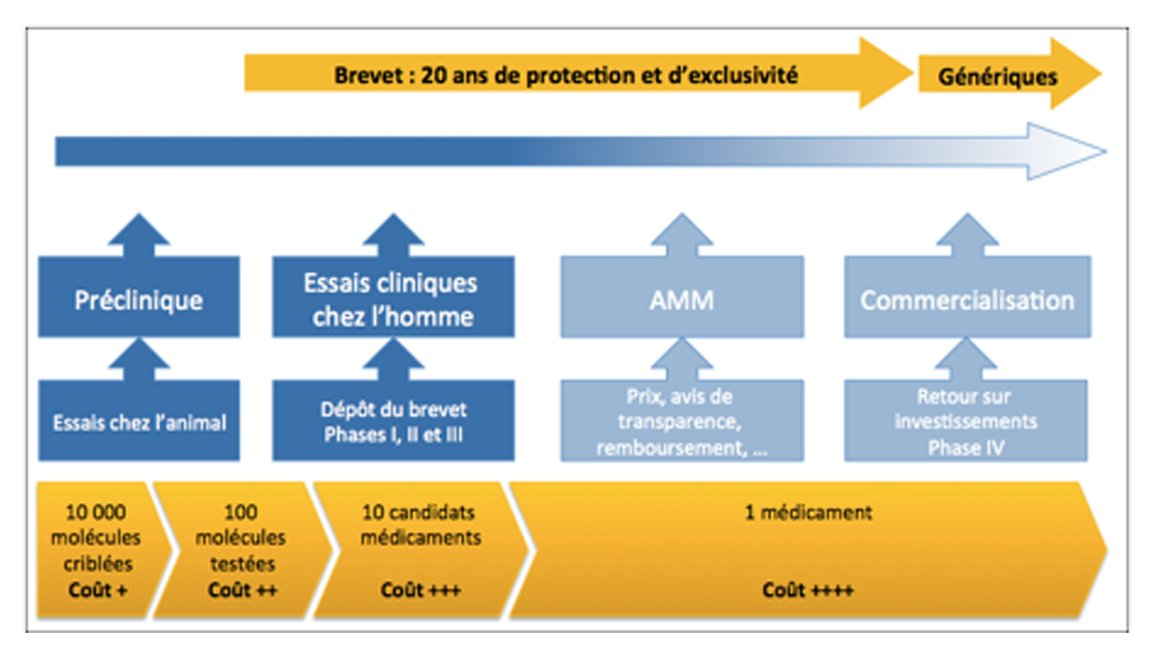
La réglementation des essais
La recherche clinique est très encadrée du point de vue réglementaire, notamment par les différentes lois sur le sujet. Les conditions maximales de sécurité et de rigueur scientifique sont mises en place pour s’assurer de la validité des résultats (qui ne doivent laisser aucun doute), mais surtout pour la sécurité des personnes participantes. Notamment, la loi établit que le consentement écrit, libre et éclairé des personnes doit être recueilli avant de pouvoir participer à une recherche clinique ; par ailleurs, toute personne incluse dans un essai clinique a tout liberté de retirer son consentement, et donc de ne plus participer, sans avoir à se justifier et sans que sa prise en charge, ni la relation avec son médecin, ne soit modifiée.
Quel est l'intérêt pour le patient de participer à un essai à l’Institut Godinot?
Entrer dans un essai de phase 2 ou 3 qui sont pratiqués à l’Institut peut présenter trois intérêts principaux :
- Participer à un essai peut permettre au patient qui l’accepte d’accéder à un traitement innovant.
- Cette démarche peut être bénéfique pour sa prise en charge. En effet, du fait des exigences de l'étude, les visites médicales et les examens sont plus fréquents.
- En participant à un essai, le patient devient acteur de la recherche. Il contribue aux progrès de la recherche, à l’amélioration d’un traitement. Grâce à son engagement, les informations apportées par l'essai bénéficieront à tous les malades atteints du même cancer que vous.
A la fin des essais cliniques, l’ensemble du dossier est transmis à l’Agence du Médicament, où la Commission d’AMM statue, au vu des résultats obtenus. En cas de rapport bénéfice / risque favorable, une Autorisation de Mise sur le Marché (valable 5 ans et renouvelable par périodes de 5 ans) est accordée. Après les différents circuits administratifs, le médicament peut être disponible dans les pharmacies et les prescripteurs peuvent l’utiliser chez tous les patients relevant des indications autorisées.










